Будова білків
Теорія:
Білки є обов'язковою складовою частиною будь-якого живого організму і відіграють найважливішу роль в забезпеченні процесів життєдіяльності.
До складу білків обов'язково входять чотири хімічні елементи: Карбон, Гідроген, Оксиген і Нітроген. Багато білків містять Сульфур. До складу деяких входить Фосфор. Є білки, що містять атоми металів.
Білки — природні високомолекулярні речовини (полімери), що складаються із залишків амінокислот.
Амінокислотні залишки сполучені в макромолекулах білків пептидною групою −NH−CO− , тому білки відносять до поліпептидів.
До складу білків входять двадцять амінокислот будови NH2−C|H−COOHR .
Амінокислотні залишки сполучаються у макромолекули білків у різній послідовності. Число амінокислотних залишків в молекулах теж може бути різним. Тому різноманіття білків практично безмежно. Кожен організм на Землі має свій власний неповторний набір білків.
Амінокислотні залишки сполучаються у макромолекули білків у різній послідовності. Число амінокислотних залишків в молекулах теж може бути різним. Тому різноманіття білків практично безмежно. Кожен організм на Землі має свій власний неповторний набір білків.
Білкові молекули можуть містити від одного до декількох сотень і навіть тисяч амінокислотних залишків, тому їх відносні молекулярні маси змінюються від десятків тисяч до декількох мільйонів. Так, відносна молекулярна маса гемоглобіну дорівнює: 68000 , яєчного білка — 44000 , а вірусу грипу — 32000000 .
Властивості білка в першу чергу визначаються порядком сполучення амінокислотних залишків у поліпептидному ланцюгу.
Послідовність амінокислотних залишків в макромолекулі називається первинною структурою білка.
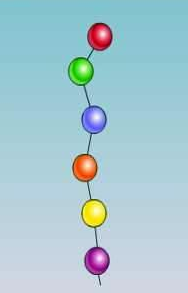
Первинна структура
Існують вторинна (спіраль) і третинна (клубок) структури білкових молекул. Вони утворюються в результаті внутрішньомолекулярної взаємодії частин поліпептидного ланцюга.
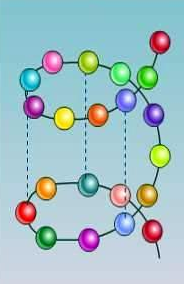
Вторинна структура
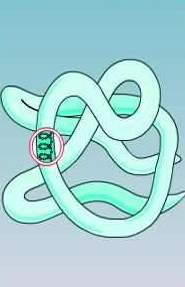
Третинна структура
Кілька білкових молекул можуть сполучатися одна з одною і утворювати четвертинну структуру.
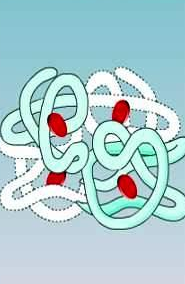
Четвертинна структура
Властивості і функції білків
Теорія:
Властивості білків
Розчиність
За здатністю розчинятися білки діляться на розчинні і нерозчинні. До розчинних відноситься білок курячого яйця. Не можуть розчинятися білки вовни, пір'я, нігтів.
Гідроліз
При дії води в присутності кислоти або ферментів білки піддаються гідролізу. В результаті розщеплення білкових молекул водою утворюється суміш амінокислот. Такий процес відбувається в органах травлення при перетравленні білкової їжі. Утворені амінокислоти всмоктуються в кров і використовуються організмом для синтезу власних білків.
Денатурація
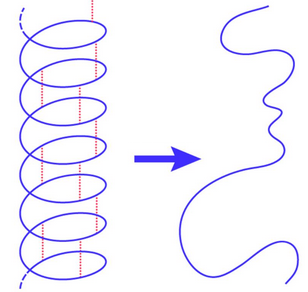
Денатурація — руйнування просторової структури білка.
Вона відбувається при нагріванні білків, під дією радіоактивного випромінювання, деяких хімічних речовин (кислот, лугів, солей важких металів). При денатурації білки змінюють свої властивості і втрачають біологічну активність, незважаючи на те, що їх первинна структура зберігається.
Прикладом денатурації служить зміна яєчного білка при нагріванні.
Розклад при нагріванні
При сильному нагріванні білки горять. При цьому утворюються речовини зі своєрідним запахом паленого пір'я. По запаху можна легко відрізнити вовняні або шовкові волокна від синтетичних.
Кольорові реакції
Присутність білка у розчині можна виявити за допомогою якісних реакцій, в результаті яких утворюються забарвлені продукти.
Якщо до розчину білка додати розчин лугу і кілька крапель розчину солі купрум(

Інша кольорова реакція на білки — ксантопротеїнова. Для її проведення до розчину білка при нагріванні треба додати концентровану нітратну кислоту. Утворюється жовтий осад. Якщо після охолодження в пробірку долити розчин лугу або концентрований розчин аміаку, то з'явиться оранжеве забарвлення.

Функції білків
У кожному живому організмі міститься велика кількість білків, які виконують ряд найважливіших функцій.
Білки входять до складу цитоплазматичної мембрани, цитоплазми, органоїдів і тим самим виконують будівельну функцію в живих організмах.
Всі біохімічні реакції в організмах протікають за участю ферментів. Ферменти — це білки-каталізатори. Отже, білки в живих організмах виконують каталітичну функцію. Прикладами таких каталізаторів можуть бути травні ферменти, що беруть участь в перетравленні їжі: пепсин, ліпаза, амілаза, мальтаза.
Найважливіша функція білків — захисна. Особливі білки — антитіла і антитоксини — беруть участь у формуванні імунітету. Антитіла знешкоджують бактерії, що проникли в організм, а антитоксини нейтралізують їх отрути.
Білок гемоглобін виконує транспортну функцію. Він переносить кисень від органів дихання до тканин.
Рухова функція деяких білків забезпечує скорочення м'язів і всі рухи живих організмів.
При нестачі їжі білки можуть виконувати енергетичну функцію. При розщепленні
Білки виконують сигнальну, рецепторну, регуляторну та інші функції.
Лабораторна робота 6. Кольорові реакції білків
Мета роботи: дослідити денатурацію білка під впливом різних чинників,
ознайомитися з кольоровими реакціями білків, які є якісними реакціями.
Хід роботи
Дослід 1. Денатурація білка.
У п'ять пробірок налийте по 1 мл розчину білка курячого яйця.
У першу пробірку додайте 1 мл етилового спирту, у другу — 1 мл розчину
купрум(ІІ) сульфату, у третю — 1 мл розчину лугу або кислоти,
вміст четвертої пробірки нагрійте у полум'ї спиртівки, вміст п'ятої
пробірки енергійно збовтайте. Які спільні ознаки змін, що відбуваються
у кожній з пробірок? У яких випадках денатурація відбувається більш, а
у яких менш інтенсивно? Чим відрізняється зворотна денатурація від
незворотної?
Дослід 2. Біуретова реакція. Виявлення пептидного зв'язку у молекулах
білка.
- Біуретова реакція використовується для виявлення пептидного зв'язку
- в молекулах білків.
У дві пробірки налийте 1 мл розчину натрій гідроксиду та додайте у кожну
по 2 краплі розчину купрум(II) сульфату. Що спостерігаєте?
Поясніть спостереження, напишіть рівняння реакції. У першу пробірку
додайте 1 мл води, у другу — 1 мл розчину білка курячого яйця.
Обидві пробірки енергійно збовтайте. Що спостерігаєте? Зробіть висновок.
Дослід 3. Ксантопротеїнова реакція.
- Ксантопротеїнова реакція дозволяє виявити в молекулах білків циклічні
- амінокислоти, які містять ароматичне ядро.
Налийте в пробірку розчин білка курячого яйця об'ємом 1 мл, добавте 0,5 мл
концентрованої нітратної кислоти і обережно нагрійте. Що спостерігаєте? є
Охолодіть вміст пробірки, по краплях додайте розчин амоніаку до зміни забарвлення.
Немає коментарів:
Дописати коментар