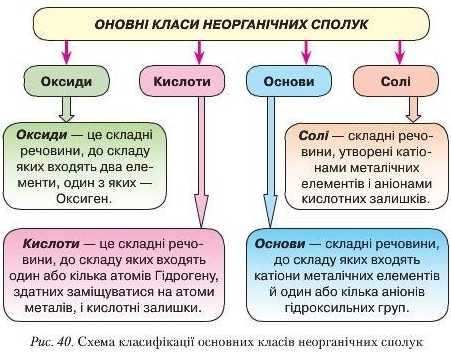
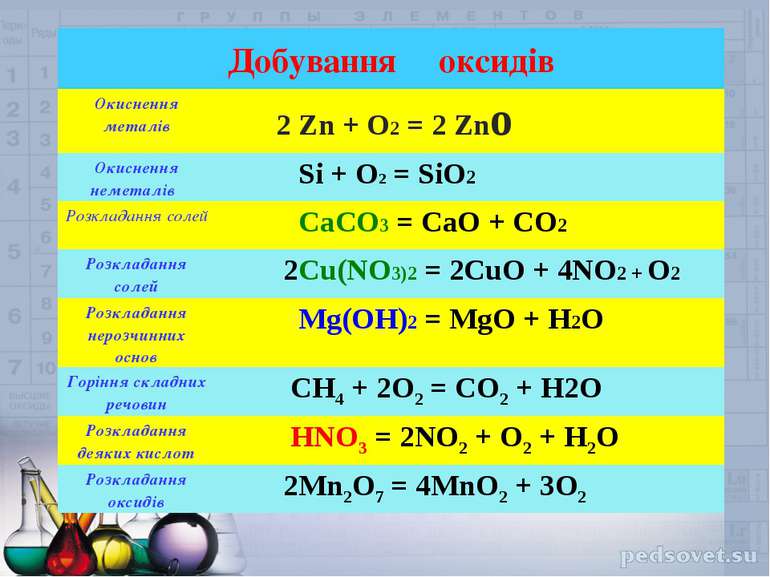
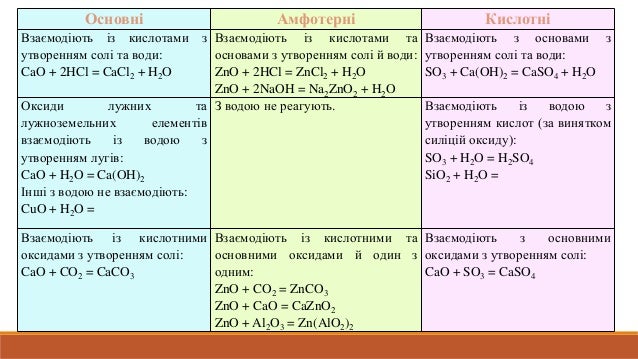
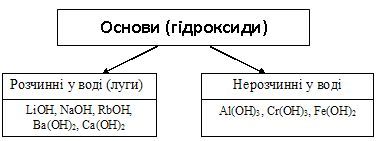
Підсумкова контрольна робота
піготовка
(завдання будуть подібні)
Варіант І
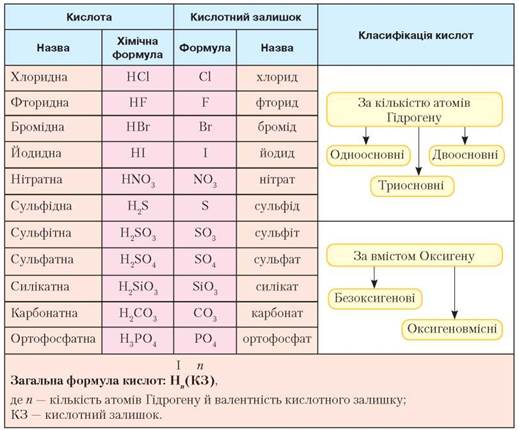
1. Дано ряд речовин: Назвіть ці речовини.
Ca(NO3)2 _____________________________________
H2SO4 ________________________________________
SiO2 __________________________________________
Al(OH)3 _______________________________________
CaО _________________________________________
FeSO4 _______________________________________
P2O5 ________________________________________
CaCO3 ______________________________________
H2CO3 ______________________________________
2. Виберіть із переліку речовини, розчини яких забарвлюють фенолфталеїн у малиновий колір:
1) NaOH; 2) Na2SO4; 3) HCl; 4) CaCO3.
3. Установіть відповідність:
а) кислотний оксид 1) SO3
б) основний оксид 2) Na2S
в) амфотерний оксид 3) CaО
г) не є оксидом 4) ZnО
4. Виберіть речовину, що не буде взаємодіяти із сульфатною кислотою:
а) Hg; б)Na2SO4; в)Zn; г)Cu(OH)2.
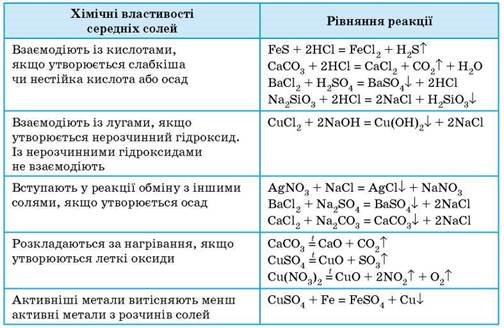
5. Виберіть ряд солей, розчини яких унаслідок у взаємодії з розчином NaOH утворюють виключно нерозчинні основи:
1) NaCl, CuCl2, MgCl2;
2) Al2(SO4)3, CuSO4, Na2SO4;
3) AlCl3, CuCl2, MgCl2.
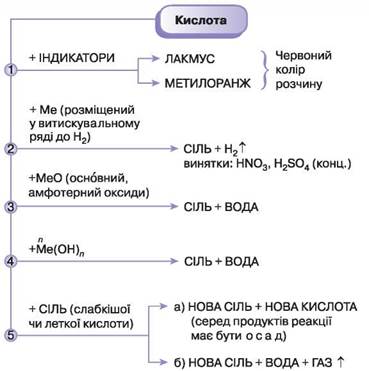
6. Допишіть рівняння можливих реакцій:
1) CO2 +NaOH → 2) Cu + ZnSO4→
3) Na2SO4 +H2CO3 → 4) H2S+KOH→
7. Для нейтралізації хлоридної кислоти кількістю речовини 0,5 моль
необхідно взяти кальцій гідроксид кількістю речовини:
а) 0,5 моль; б) 0,25 моль; в) 1 моль; г) 1,5 моль.
8. Здійсніть перетворення: Ca→CaO→Ca(OH)2→CaCl2
9. До розчину арґентум нітрату додали 55г натрій хлориду. Яка маса осаду при цьому утвориться?
Варіант ІІ
1. Дано ряд речовин, Назвіть ці речовини.
KOH _________________________________
SO3 _________________________________
KNO3 _________________________________
HNO3 _________________________________
FeО _________________________________
Na2SO4 _________________________________
Al(OH)3 _________________________________
H3PO4 _________________________________
MgCl2 _________________________________
2. Виберіть із переліку речовини, розчини яких забарвлюють метиловий оранжевий у жовтий колір:
1) H2SO4; 2) H2CO3; 3) NaCl; 4) Ba(OH)2.
3. Установіть відповідність:
а) безоксигенова кислота 1) Cu(OH)2
б) оксигеновмісна кислота 2) HCl
в) сіль 3) Na2SO4
г) основа 4) H3PO4
4. Виберіть речовину, що не буде взаємодіяти із сульфатною кислотою:
а)SO2; б)Ag; в)Al; г)Al(OH)3.
5. Виберіть ряд, у якому всі оксиди внаслідок розчинення у воді утворюють луги:
1) Na2O, BaО, K2O;
2) Na2O, Cu2O, N2O;
3) CO, BaО, CaО.
6. Допишіть рівняння можливих реакцій:
1) Cu(OH)2+NaOH→ 2) Fe +CuSO4→
3) BaO+KOH→ 4) Zn +HCl→
7. Для нейтралізації сульфатної кислоти кількістю речовини 1 моль необхідно
взяти натрій гідроксид кількістю речовини:
а) 1 моль; б) 2 моль; в) 0,5 моль; г) 4 моль.
8. Здійсніть перетворення:
1) K2O→ KOH→ KNO3
2) KOH→K2SO4
9. До розчину сірчаної кислоти додали 33,6 г калій гідроксиду. Скільки грамів солі при цьому утворюється?
Урок 1-2