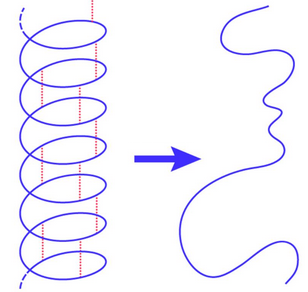
Склад і класифікація вуглеводів
Теорія:
Вуглеводи — природні оксигеновмісні сполуки. До їх складу входять три елементи: Карбон, Гідроген і Оксиген. Співвідношення числа атомів Гідрогену і Оксигену таке ж саме, як у воді — 2 : 1 . Звідси і пішла назва «вуглеводи».
У загальному вигляді склад більшості вуглеводів можна виразити формулою Cn(H2O)m .
Вуглеводи входять до складу клітин всіх живих організмів.
Особливо високий вміст вуглеводів у рослинах. Клітинні стінки рослин утворені целюлозою. Вона є основною складовою частиною деревини. Майже чистою целюлозою є вата.

Найважливіша запасна речовина рослин — крохмаль. Він у великих кількостях міститься в насінні злаків, в бульбах картоплі. Солодкий смак фруктам і овочам надають глюкоза, фруктоза, сахароза.
Сумішшю вуглеводів є мед.

Запасною речовиною в клітинах грибів і тварин є глікоген (тваринний крохмаль). У крові тварин і людини міститься глюкоза, яка служить основним джерелом енергії для всіх процесів, що протікають в організмі.
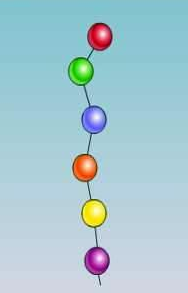
Вуглеводи поділяють на три групи: моносахариди, дисахариди і полісахариди. В основі такого поділу лежить здатність молекул вуглеводів піддаватися гідролізу.
Молекули моносахаридів у водних розчинах гідролізу не піддаються і не змінюються.
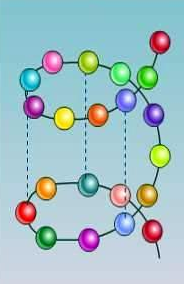
Молекули дисахаридів розкладаються водою на дві молекули моносахаридів.
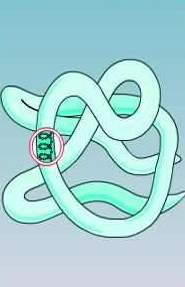
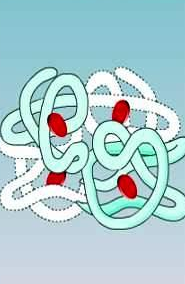
При гідролізі полісахаридів з однієї молекули утворюється багато молекул моносахаридів.
Моносахариди
Теорія:
Прості вуглеводи відносяться до групи моносахаридів. Моносахариди відрізняються від інших груп вуглеводів відсутністю реакції гідролізу. Вони не реагують з водою і не розкладаються на простіші речовини.
Згадаємо властивості двох шестикарбонових моносахаридів: глюкози і фруктози. Склад молекул цих речовин однаковий і виражається формулою:
Глюкоза
Глюкоза — найпоширеніший у природі моносахарид. Вона утворюється рослинами в процесі фотосинтезу з вуглекислого газу і води:

 .
.
Глюкоза зустрічається у всіх органах рослин, в стиглих фруктах і ягодах. Багато її міститься у винограді, тому глюкозу називають ще виноградним цукром.
Глюкоза знаходиться і в організмах тварин. У крові людини її міститься приблизно
Глюкоза є білою кристалічною речовиною, добре розчинна у воді, солодка на смак.
Встановлено, що в природі глюкоза існує в лінійній і циклічній формах, які здатні до взаємоперетворення. Тому її будову виражають не одною, а трьома структурними формулами.
Циклічні форми глюкози відрізняються розташуванням гідроксильних груп у першого атому Карбону (виділені на малюнку).
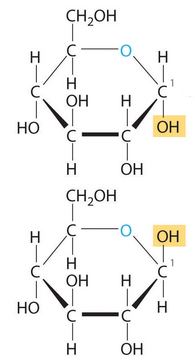
Молекула глюкози в лінійній формі містить п'ять гідроксильних груп і одну альдегідну групу. Функціональні групи визначають характерні хімічні властивості глюкози: для неї характерні як реакції багатоатомних спиртів, так і реакції альдегідів.
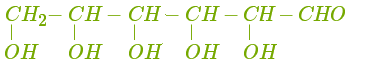
Одна з властивостей глюкози — взаємодія з купрум(II ) гідроксидом. При кімнатній температурі глюкоза зі свіжоприготованим гідроксидом утворює прозорий яскраво-синій розчин (реакція багатоатомних спиртів).

При нагріванні глюкози з аміачним розчином аргентум оксиду на стінках пробірки з'являється блискучий наліт — «срібне дзеркало» (реакція альдегідів).

Для глюкози характерні також особливі реакції, які протікають в клітинах живих організмів. Це реакції бродіння. В результаті бродіння, в залежності від умов протікання, можуть утворюватися різні продукти.
Під впливом ферментів дріжджів відбувається спиртове бродіння. Утворюються етиловий спирт і вуглекислий газ:
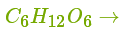
 .
.
Цей процес використовується у приготуванні дріжджового тіста, у виноробстві, пивоварінні.
Під впливом ферментів молочнокислих бактерій глюкоза перетворюється у молочну кислоту:
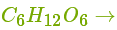
 .
.
Молочнокисле бродіння використовується для отримання кислого молока, кефіру, сиру, сметани.
У клітинах живих організмів глюкоза є головним джерелом енергії для всіх життєвих процесів. В живому організмі відбувається повільне окиснення глюкози з утворенням вуглекислого газу і води. При цьому виділяється енергія:

 .
.
Глюкоза використовується у медицині як поживна речовина і складова частина протишокових рідин. Застосовується вона для отримання лимонної кислоти, вітамінів С і Н.
Знаходить глюкоза застосування і у кондитерській промисловості при виготовленні мармеладу, пряників, карамелі; у виробництві молочної кислоти, етанолу.
Отримують глюкозу гідролізом полісахаридів: крохмалю або целюлози.
Сахароза
Теорія:
Дисахариди — вуглеводи, при гідролізі яких їх молекула розпадається на дві молекули моносахаридів.
Загальна формула дисахаридів — C12H22O11 . Найвідоміший дисахарид — сахароза, чи буряковий цукор.
Сахароза широко поширена в рослинному світі. Вона міститься в соку всіх рослин. Особливо багато її в коренеплодах цукрового буряка, в стеблах цукрової тростини, в соку цукрового клена. Ці рослини спеціально вирощують, щоб отримувати з них сахарозу.

Цукрова тростина

Цукровий буряк
Сахароза — кристалічна речовина, добре розчинна у воді, солодка на смак.
Вона піддається гідролізу, тобто розкладанню водою. Якщо до розчину сахарози додати розчин сульфатної кислоти і суміш прокип'ятити, то утворюється суміш двох моносахаридів — глюкози і фруктози. Тому сахарозу відносять до дисахаридів.
При нагріванні сахароза легко плавиться, обвуглюється, але не горить. Проте, суміш цукрового пилу з повітрям може вибухати.
Використовується сахароза в харчуванні для надання продуктам солодкого смаку. В організмі вона розщеплюється на глюкозу і фруктозу і в такому вигляді потім засвоюється.

Вживання занадто великої кількості цукру може привести до серйозних порушень обміну речовин і викликати цукровий діабет.