Окисно-відновні реакції
Теорія:
Окисно-відновними реакціями називаються хімічні реакції, які протікають зі зміною ступенів окиснення атомів хімічних елементів або йонів, що утворюють реагуючі речовини.
Загальна схема окисно-відновної реакції (ОВР) виглядає наступним чином:
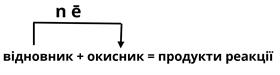
Зверни увагу!
Відбуваються одночасно два процеси: окиснення і відновлення.
Приклад:
Розглянемо схему ОВР взаємодії заліза з хлоридною кислотою:
При цьому катіон Гідрогену приймає електрони:
атом Феруму віддає електрони:
Таким чином, у даній реакції йон Гідрогену є окисником, сам при цьому відновлюється. Відбувається процес відновлення Гідрогену до простої речовини. Ступінь відновлення атомів Гідрогену знижується.
Залізо є відновником. Відбувається окиснення атомів Феруму, його ступінь окиснення підвищується.
Copyright © 2021 МiйКлас
Теорія:
Складання рівнянь окисно-відновних реакцій (ОВР) з розстановкою коефіцієнтів простим підбором, як правило, викликає певні труднощі.
Для складання рівнянь ОВР використовують метод електронного балансу.
Метод базується на тому, що в ОВР дотримується правило:
загальне число електронів, відданих відновником, дорівнює загальній кількості електронів, прийнятих окисником.
Щоб скласти рівняння ОВР методом електронного балансу потрібно:
- записати схему реакції;
- вказати ступені окиснення і визначити елементи, які змінюють ступінь окиснення;
- скласти рівняння процесів окиснення і відновлення;
- зрівняти число приєднаних та відданих електронів, ввівши множники, використавши найменше спільне кратне;
- підставити знайдені коефіцієнти перед формулами речовин, що містять ці частинки;
- розставити коефіцієнти перед формулами інших речовин методом підбору;
- перевірити правильність розстановки коефіцієнтів.
Приклад:
При взаємодії гідроген сульфіду з киснем йон Сульфуру і атоми Оксигену змінюють ступені окиснення, записуємо рівняння процесу окиснення Сульфуру і відновлення Оксигену:
Найменше спільне кратне (НСК) дорівнює 12 . Відповідно коефіцієнт перед гідроген сульфідом — 2 ; перед киснем — 3 .
Правильність розстановки коефіцієнтів перевіримо за числом атомів Оксигену. У лівій і у правій частині рівняння міститься по 6 атомів Оксигену.


Немає коментарів:
Дописати коментар